โครงสร้างสามมิติของเอนไซม์แอสปาร์ทิลทีอาร์เอ็นเอซินทิเทสจากแบคทีเรีย Helicobacter pylori
โปรตีนเป็นเป็นสารชีวโมเลกุลซึ่งมีความสำคัญในเซลล์สิ่งมีชีวิต ดังนั้นกระบวนการสังเคราะห์โปรตีนในเซลล์สิ่งมีชีวิตจึงมีความสำคัญอย่างยิ่ง ความถูกต้องของการสังเคราะห์โปรตีนในเซลล์ขึ้นอยู่กับกระบวนการเชื่อมต่อกรดอะมิโนแต่ละชนิดกับทีอาร์เอ็นเอที่ถูกต้องอย่างจำเพาะเจาะจง ซึ่งเอนไซม์แอสปาร์ทิลทีอาร์เอ็นเอซินทิเทสจะจับกับแอนติโคดอนของทีอาร์เอ็นเอ โดเมนด้านปลายอะมิโน (N-terminus) ของเอนไซม์ จะทำหน้าที่ต่อกรดอะมิโนที่ถูกต้องเข้ากับทีอาร์เอ็นเอด้วยพันธะโควาเลนท์ จากนั้นกรดอะมิโนแต่ละตัวจะต่อกันเป็นสายโพลีเปบไทด์
จากความสำคัญของเอนไซม์แอสปาร์ทิลทีอาร์เอ็นเอซินทิเทสต่อกระบวนการสังเคราะห์โปรตีนในเซลล์สิ่งมีชีวิต รศ. ดร. พิทักษ์ เชื้อวงศ์ อาจารย์ประจำภาควิชาเคมี คณะวิทยาศาสตร์ มหาวิทยาลัยเกษตรศาสตร์ บางเขน จึงสนใจศึกษาคุณสมบัติและโครงสร้างโปรตีนแอสปาร์ทิลทีอาร์เอ็นเอซินทิเทส คณะวิจัยสามารถผลิตโปรตีนแอสปาร์ทิลทีอาร์เอ็นเอซินทิเทสส่วนที่จับกับแอนติโคดอนของทีอาร์เอ็นเอ โปรตีนแอสปาร์ทิลทีอาร์เอ็นเอซินทิเทสที่ศึกษาเป็นโปรตีนจากแบคทีเรีย Helicobacter pylori ซึ่งเป็นแบคทีเรียแกรมลบและก่อโรคในมนุษย์ การติดเชื้ออาจทำให้เกิดโรคแผลในกระเพาะอาหาร รวมถึงมะเร็งกระเพาะอาหารด้วย
คณะวิจัยได้ผลิตโปรตีนบริสุทธิ์ ผลการวิเคราะห์โดยเทคนิค Dynamic light scattering พบว่าโปรตีนมีความเสถียรในช่วงอุณหภูมิที่ทดสอบระหว่าง 20 ถึง 42 องศาเซลเซียส คณะวิจัยสนใจศึกษาโครงสร้างของเอนไซม์ดังกล่าวเพื่อนำไปสู่ความเข้าใจกลไกการเร่งปฏิกริยา เทคนิค Circular dichroism spectroscopy ให้ข้อมูลโครงสร้างแบบแผ่นพับซ้อนซึ่งมีความเสถียรที่อุณหภูมิสูง ซึ่งสอดคล้องกับผลการทดลองจากเทคนิค Nuclear Magnetic Resonance Spectroscopy
ในการวิเคราะห์โครงสร้างสามมิติของเอนไซม์ ด้วยเทคนิค Macromolecular X-ray Crystallography ดร. ชมภูนุช ส่งสิริฤทธิกุล นักวิทยาศาสตร์ระบบลำเลียงแสงของสถาบันวิจัยแสงซินโครตรอนได้เตรียมผลึกของโปรตีนแอสปาร์ทิลทีอาร์เอ็นเอซินทิเทสในสารละลายที่ประกอบด้วยแอมโมเนียมซัลเฟต บัฟเฟอร์ซิเทรต และโพลีเอธิลีนไกลคอล 4,000 ในอัตราส่วนความเข้มข้นที่เหมาะสม (รูปที่ 1A; อุณหภูมิบ่ม 18 องศาเซลเซียส เป็นเวลา 2 วัน ด้วยเทคนิค Microbatch และ 1B; อุณหภูมิบ่ม 4 องศาเซลเซียส เป็นเวลา 6 วัน ด้วยเทคนิค Vapor diffusion) ซึ่งสามารถเก็บข้อมูลการเลี้ยวเบนรังสีเอกซ์ได้ความละเอียดระดับ 2.0 อังสตรอม มี unit-cell parameters a = b = 61.83, c = 141.38 Å จัดอยู่ในกลุ่มสมมาตรแบบ tetragonal และมี space group แบบ P41212 โดยหนึ่ง asymmetric unit ประกอบด้วยโปรตีนสองโมเลกุล และมีน้ำเป็นองค์ประกอบ 57.83%


รูปที่ 1 ผลึกของเอนไซม์แอสปาร์ทิลทีอารีเอ็นเอซินทิเทสจากแบคทีเรีย H. Pylori 1A) เตรียมได้ในเบื้องต้นด้วยเทคนิค Microbatch 1B) เตรียมได้โดยปรับสภาวะการทดลองจาก 1A) ด้วยเทคนิค Vapor diffusion
โครงสร้างโปรตีนเป็นแบบ Oligonucleotide/Oligosaccharide-Binding (OB) fold (รูปที่ 2) เมื่อเปรียบเทียบโครงสร้างสามมิติของเอนไซม์จากแบคทีเรีย H. Pylori กับแบคทีเรียอื่นๆ พบว่ามีความคล้ายทั้งรูปร่างและขนาด (รูปที่ 3) แต่มีโครงสร้าง turn ที่แตกต่างกัน ซึ่งส่งผลให้เอนไซม์จากแบคทีเรีย H. Pylori มีโครงสร้างที่ compact มากกว่า นอกจากนี้ด้วยคุณสมบัติของ turn E และ turn F ทำให้เอนไซม์สามารถจับได้ทั้งแอนติโคดอนของทีอาร์เอ็นเอชนิด tRNAAsp (34GUC36) และ tRNAAsn (34GUU36) ซึ่งโครงสร้างที่วิเคราะห์ได้บ่งชี้ว่ากรดอะมิโนโพรลีนตำแหน่งที่ 84 มีความสำคัญที่น่าจะมีผลต่อความจำเพาะของเอนไซม์
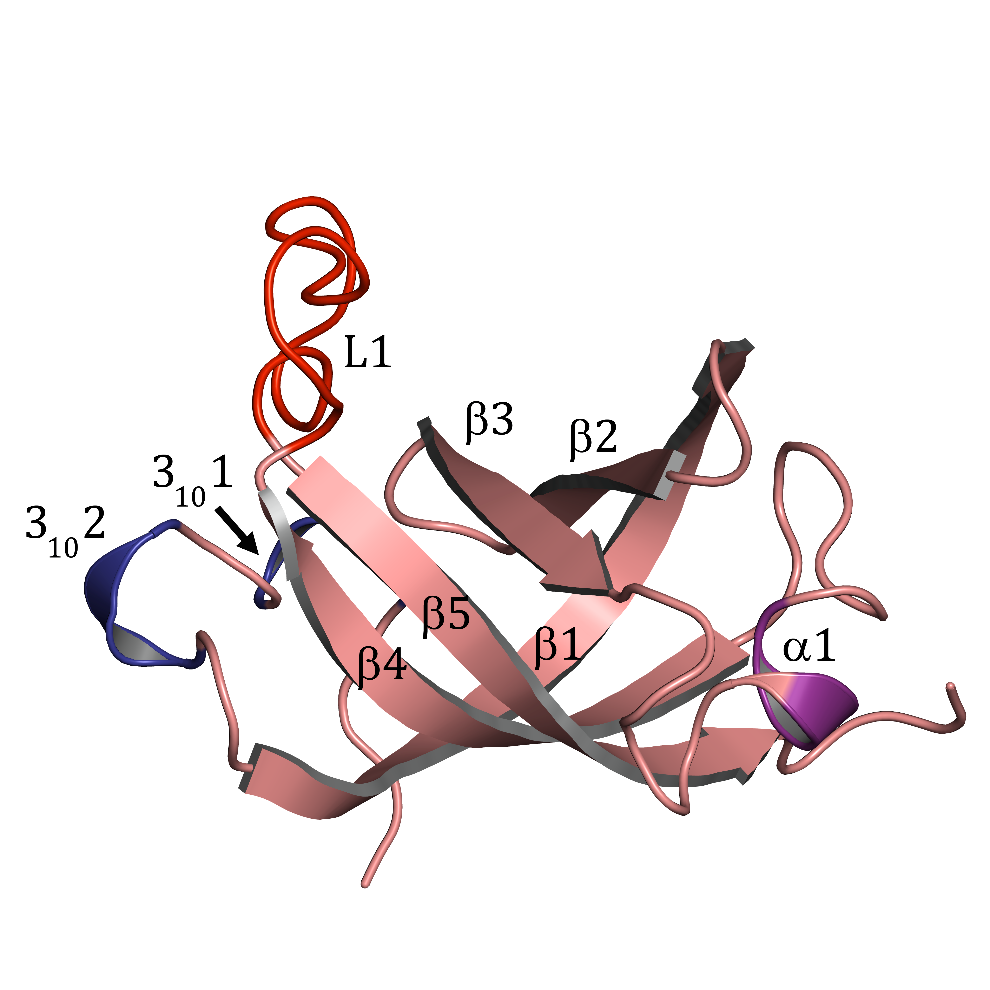
รูปที่ 2 โครงสร้างสามมิติของเอนไซม์แอสปาร์ทิลทีอาร์เอ็นเอซินทิเทสจากแบคทีเรีย H. Pylori (PDB code 5GRO)
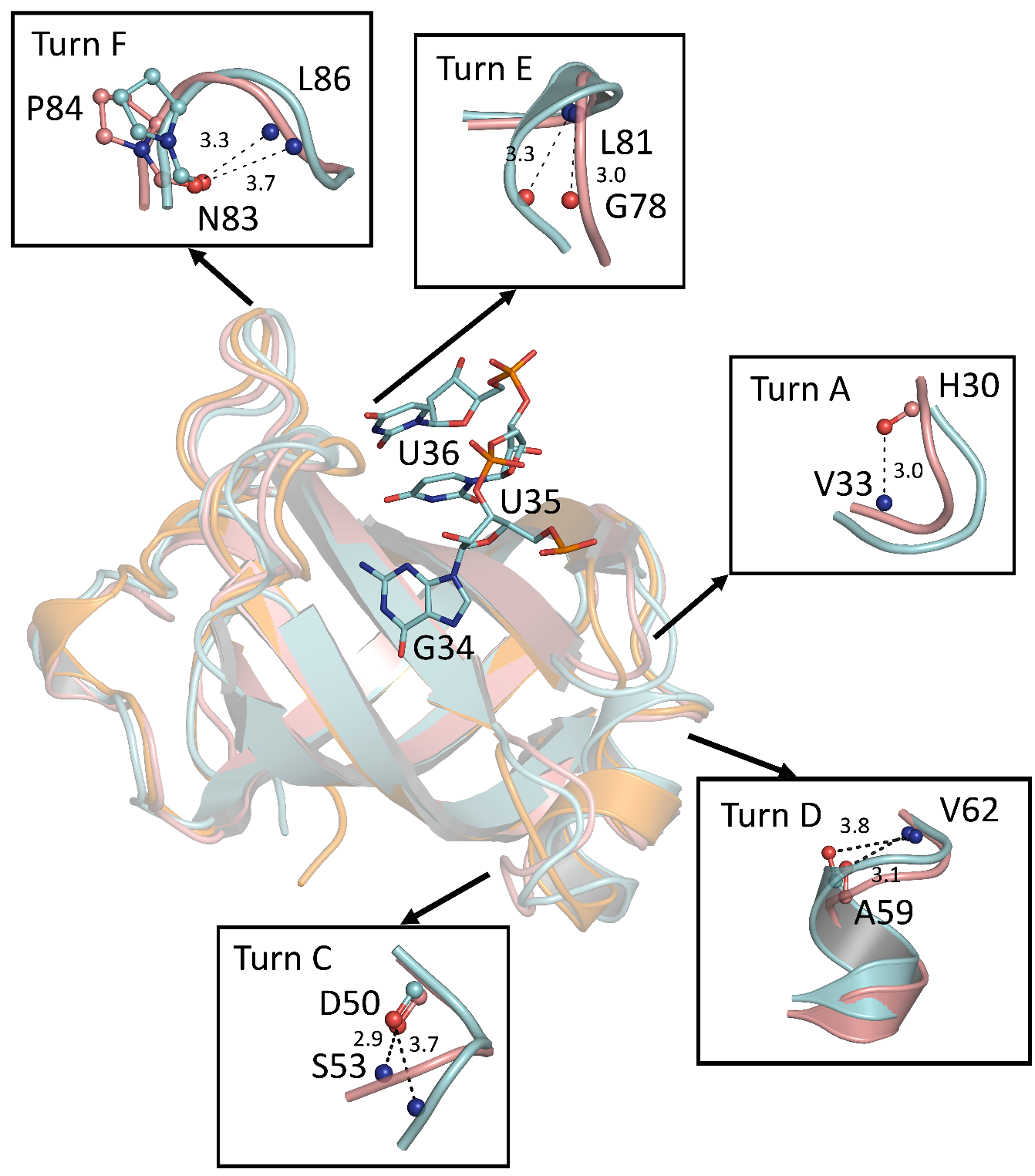
รูปที่ 3 โครงสร้างสามมิติของเอนไซม์แอสปาร์ทิลทีอาร์เอ็นเอซินทิเทสจากแบคทีเรีย H. Pylori (PDB code 5GRO; สีชมพูส้ม) เปรียบเทียบกับโครงสร้างจากแบคทีเรีย Pseudomonas aeruginosa (สีฟ้าเขียว) และจากแบคทีเรีย Mycobacterium smegmatis (สีส้ม)
คณะผู้วิจัย
ดร. ชมภูนุช ส่งสิริฤทธิกุล สถาบันวิจัยแสงซินโครตรอน (องค์การมหาชน) และศูนย์โครงสร้างและฟังก์ชั่นการประยุกต์ใช้ชีวโมเลกุล
พิชญดา เฟื่องฟูลอย, สุวิมล สืบค้า และรศ. ดร. พิทักษ์ เชื้อวงศ์ คณะวิทยาศาสตร์ มหาวิทยาลัยเกษตรศาสตร์ บางเขน
Prof. Dr. Chun-Jung Chen, Scientific Research Division, National Synchrotron Radiation Research Center, Hsinchu, Taiwan
เอกสารอ้างอิง
- Songsiriritthigul, C., Suebka, S., Chen, C-J., Fuengfuloy, P. & Chuawong, P. (2017) Crystal structure of the N-terminal anticodon-binding domain of non-discriminating aspartyl-tRNA synthetase from Helicobacter pylori. Acta Crystallographica F: Structural Biology Communications. F73, 62-69.
- Fuengfuloy, P., Chuawong, P., Suebka, S., Wattana-amorn, P., Williams, C., Crump, P. M. & Songsiriritthigul, C. (2013). Overproduction of the N-terminal anticodon-binding domain of the non-discriminating aspartyl-tRNA synthetase from Helicobacter pylori for crystallization and NMR Measurements. Protein Expression and Purification. 89(1), 25-32. DOI: 10.1016/j.pep.2013.02.006.
- Chuawong, P. & Hendrickson, T. L. (2006). The nondiscriminating aspartyl-tRNA synthetase from Helicobacter pylori: anticodon-binding domain mutations that impact tRNA specificity and heterologous toxicity. Biochemistry. 45, 8079-8087.

















