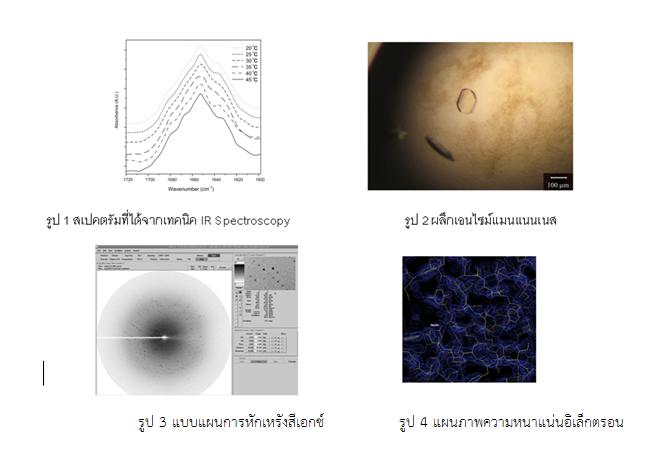
เอนไซม์แมนแนนเนสเป็นเอนไซม์ในกลุ่มไกลโคซิลไฮโดรเลส (GH26) ซึ่งมีคุณสมบัติในการเร่งปฏิกริยาการย่อยโมเลกุลน้ำตาลสายยาวซึ่งพบมากในหัวบุกและกากมะพร้าว ให้ได้ผลิตภัณฑ์ที่เป็นน้ำตาลสายสั้นลงสามารถนำไปใช้ประโยชน์ในอุตสาหกรรมการผลิตอาหารและอาหารเสริม ซึ่งมีประโยชน์ในเชิงการเพิ่มมูลค่าของวัตถุดิบการเกษตร
คณะผู้วิจัยประสบความสำเร็จในการผลิตเอนไซม์แมนแนนเนสที่บริสุทธิ์จากแบคทีเรีย Bacillus licheniformis และทดสอบคุณสมบัติการเร่งปฏิกริยาที่สภาวะต่างๆ พบว่าเอนไซม์ทำงานได้ดีที่ pH 6.0-7.0 และอุณหภูมิ 50-60 องศาเซลเซียส ซึ่งเป็นสภาวะที่เหมาะสมในการประยุกต์ใช้จริงในระดับอุตสาหกรรม จากการวิเคราะห์ผลผลิตที่ได้จากการย่อยโมเลกุลน้ำตาลของเอ็นไซม์ พบว่าเอนไซม์มีความจำเพาะในการเร่งปฏิกริยาของสารตั้งต้นโมเลกุลน้ำตาลชนิดต่างๆ แตกต่างกัน นอกจากนั้นได้ทำการตรวจสอบคุณสมบัติโครงสร้างหน่วยย่อยและน้ำหนักโมเลกุลเอนไซม์ด้วยเทคนิค MALDI-TOF Mass Spectrometry รวมถึงวิเคราะห์การเปลี่ยนแปลงโครงสร้างทุติยภูมิของเอนไซม์ที่อุณหภูมิต่าง ๆ ด้วยเทคนิค Infrared Spectroscopy ที่สถานีทดลอง IR Spectroscopy and Imaging ณ สถาบันวิจัยแสงซินโครตรอน (องค์การมหาชน) พบว่าโครงสร้างทุติยภูมิของเอนไซม์ เริ่มมีการเปลี่ยนแปลง ทีอุณหภูมิ 40-45oC แต่อย่างไรก็ตามไม่พบการเปลี่ยนแปลงโครงสร้างในระดับที่ทำให้โปรตีนสูญเสียคุณสมบัติ ซึ่งผลที่ได้ผลสอดคล้องกับการศึกษาผลของอุณหภูมิต่อคุณสมบัติความเสถียรของเอนไซม์
เพื่อนำไปสู่ความเข้าใจกลไกการเร่งปฏิกริยาของเอนไซม์ให้ดีขึ้น จึงได้เตรียมผลึกเอนไซม์ดังกล่าว ณ ห้องปฏิบัติการสถาบันวิจัยแสงซินโครตรอน และเก็บข้อมูลการหักเหรังสีเอกซ์โดยเครื่อง X-ray diffractometer ณ ปลายสถานีทดลอง Macromolecule Crystallography (MX) ของสถาบันวิจัยแสงซินโครตรอน ซึ่งแบบแผนการหักเหรังสีเอกซ์ที่ระดับความแยกแยะ 2.3 อังสตรอม ได้ถูกนำไปประมวลผลเพื่อหากลุ่มสมมาตรและขนาด unit cell ของผลึกซึ่งสามารถหาเฟสเริ่มต้นเพื่อวิเคราะห์โครงสร้างสามมิติของเอนไซม์ได้
ดร. ชมภูนุช ส่งสิริฤทธิกุล ดร. วราภรณ์ ตัณฑนุช และศศิธร ลาภบุญเรือง
สถาบันวิจัยแสงซินโครตรอน (องค์การมหาชน)
ดร. สิทธิรักษ์ รอยตระกูล
สถาบันจีโนม ศูนย์พันธุวิศวกรรมและเทคโนโลยีชีวภาพแห่งชาติ
บัญชา บูรณะบัญญัติ และรศ.ดร. มณฑารพ ยมาภัย
สาขาวิชาเทคโนโลยีชีวภาพ สำนักวิชาเทคโนโลยีการเกษตร มหาวิทยาลัยเทคโนโลยีสุรนารี
Prof. Dietmar Haltrich,
BOKU, University of Natural Resources and Applied Life Sciences, Vienna, Austria
เอกสารอ้างอิง
- 1.Songsiriritthigul, C, Lapboonrueng, S, Roytrakul, S, Haltrich, D, Yamabhai, M. Crystallization and Preliminary Crystallographic Analysis of β-Mannanase from Bacillus licheniformis. Acta Cryst. 2011; F67: 217–220.
- 2.Yamabhai M, Buranabanyat B, Jaruseranee N, Songsiriritthigul C. Efficient E. coli expression systems for the production of recombinant β -mannanases and other bacterial extracellular enzymes. Bio Bugs. 2011; 2:1, 1-5.
- 3.Songsiriritthigul, C, Lapboonrueng, S, Roytrakul, S, Haltrich, D, Yamabhai, M. Crystallization and Preliminary Crystallographic Analysis of β -Mannanase from Bacillus licheniformis. Acta Cryst. 2011; F67: 217–220.
- 4.Lapboonrueng, S, Songsiriritthigul, C, Tanthanuch, W, Roytrakul, S, Haltrich, D, Yamabhai, M. Structural analysis of β -mannanase from Bacillus licheniformis. Proceeding of The 3rd BMB International Conference “From Basic to Translational Researches for a Better Life”; The Empress Convention Centre, Chiangmai, Thailand, 6th-8th April, 2011.
- 5.Songsiriritthigul C, Buranabanyat B, Haltrich D, Yamabhai M. Efficient recombinant expression and secretion of a thermostable GH26 mannan endo-1,4- β -mannosidase from Bacillus licheniformis in Escherichia coli. Microb Cell Fact. 2010; 9(20). doi:10.1186/1475-2859-9-20.
- 6.Yamabhai M, Emrat S, Sukasem S, Pesatcha P, Jaruseranee N, Buranabanyat B. Secretion of recombinant Bacillus hydrolytic enzymes using Escherichia coli expression systems. J. Biotechnol. 2008; 133(1): 50–7.