
 Sample preparation
Sample preparation

 Sample preparation
Sample preparation
การเตรียมสารมาตรฐานเพื่อใช้ในการวิเคราะห์ด้วยเทคนิค X-ray fluorescence, XRF
การวิเคราะห์ด้วยเทคนิค X-ray fluorescence, XRF เป็นเทคนิคที่อาศัยหลักการกระตุ้นพลังงานแก่สารตัวอย่าง ซึ่งก่อให้เกิดการเปลี่ยนแปลงระดับชั้นพลังงานของอิเล็กตรอนในอะตอมสารตัวอย่าง ทำให้เกิดการคายพลังงานอยู่ในรูปของรังสีเอกซ์ เรียกว่า ฟลูออเรสเซนต์ เทคนิค XRF จะสามารถวิเคราะห์ผลได้ทั้งในเชิงคุณภาพ (Qualitative) และเชิงปริมาณ (Quantitative) โดยผลเชิงคุณภาพเกิดจากสัญญาณฟลูออเรสเซนต์มีค่าพลังงานเฉพาะธาตุ หรือมีความยาวคลื่นเฉพาะตัว จึงทำให้สามารถบ่งบอกได้ถึงชนิดธาตุในสารตัวอย่างและความเข้ม (Intensity) ของสัญญาณฟลูออเรสเซนต์สามารถบ่งบอกผลในเชิงปริมาณธาตุที่มีอยู่ในสารตัวอย่างได้ ซึ่งในการวิเคราะห์ผลเชิงปริมาณด้วยเทคนิค XRF นั้น จะสามารถทำได้โดยการสร้างกราฟปรับเทียบ (calibration curve) เพื่อหาความสัมพันธ์ระหว่างความเข้มของสัญญาณฟลูออเรสเซนต์ที่วัดได้กับปริมาณความเข้มข้นของธาตุที่อยู่ในสารมาตรฐาน โดยกราฟนี้จะสร้างขึ้นมาจากสารมาตรฐานที่ทราบค่าความเข้มข้นของธาตุที่แน่นอน เมื่อต้องการหาปริมาณความเข้มข้นของธาตุในสารตัวอย่างจะสามารถนำค่าความเข้มฟลูออเรสเซนต์ของสารตัวอย่างมาเทียบใน calibration curve ซึ่งจะทำให้ทราบค่าความเข้มข้นธาตุที่สนใจในสารตัวอย่างได้ ดังนั้นในการสร้างกราฟ calibration curve จึงจำเป็นต้องมีการเตรียมสารมาตรฐานเพื่อนำมาใช้เปรียบเทียบ ซึ่งลักษณะของสารตัวอย่างและสารมาตรฐานควรมีลักษณะเหมือนกัน กล่าวคือ ควรมีสถานะและองค์ประกอบเดียวกันในเนื้อสาร วิธีที่นิยมใช้ในการเตรียมสารมาตรฐานเพื่อใช้ในการสร้าง calibration curve จะสามารถเตรียมได้ด้วยวิธีการหลอม (fusion method) และเตรียมด้วยวิธีอัดให้เป็นเม็ด (pressed powder) ดังนั้นในการทดลองครั้งนี้จะศึกษาผลการวิเคราะห์ในเชิงคุณภาพ (Qualitative) ของสารมาตรฐานที่ถูกเตรียมด้วยวิธีต่างชนิด รวมไปถึงผลการวิเคราะห์ในเชิงปริมาณ (Quantitative) โดยจะศึกษาผลของการเตรียมสารมาตรฐานต่างวิธีที่มีผลต่อลักษณะของ calibration curve ตามลำดับ
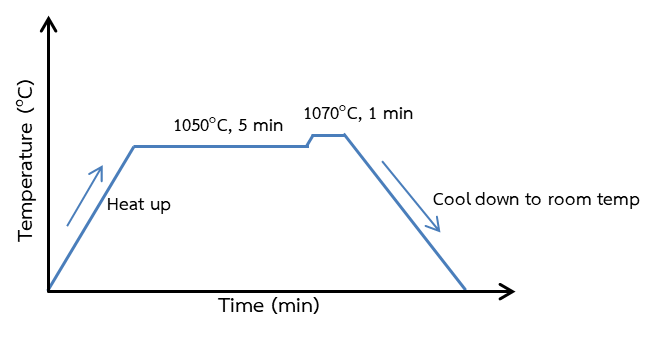
การเตรียมสารมาตรฐานเพื่อสร้าง calibration curve ที่ใช้ในการวิเคราะห์ด้วยเทคนิค XRF นั้นจะทำการเตรียมด้วยวิธีการหลอม (fusion method) ให้เป็นแก้ว (glass beads) สามารถทำได้โดยนำสารมาตรฐานมาผสมกับฟลักซ์ให้เข้ากัน แล้วนำไปหลอมที่อุณหภูมิสูง เมื่อทิ้งไว้ให้เย็นจะได้ชิ้นงานชนิดแก้วและสามารถนำไปวิเคราะห์ได้ ในขณะเดียวกัน การเตรียมสารมาตรฐานด้วยวิธีการอัด (pressed powder) ให้อยู่ในรูปเม็ด (pellet) จำเป็นต้องบดสารมาตรฐานให้ละเอียดเพื่อให้มีความเป็นเนื้อเดียวกันแล้วนำไปอัดด้วยเครื่องอัด จะได้สารตัวอย่างเป็นเม็ดหรือแผ่น แล้วนำไปวางใน kapton holder แล้วจะสามารถนำไปวิเคราะห์ได้ จากนั้นจะทำการวิเคราะห์ด้วยเทคนิค XRF เพื่อศึกษาผลของฟลูออเรสเซนต์สเปคตรัมที่เกิดขึ้น และเปรียบเทียบผล calibration curve จากการเตรียมตัวอย่างทั้งสองวิธี โดยรายละเอียด ขั้นตอน และผลการเปรียบเทียบนั้น จะถูกอธิบายดังหัวข้อถัดไป
1. สารเคมีที่ใช้ในการเตรียมสารตัวอย่าง
1.1 CaO, purity 97+% , ACROS ORGANICS
1.2 K2CO3, purity> 99% , Carlo Erba
1.3 Fe2O3, purity > 99%, SIGMA ALDRICH
1.4 Cr2O3, purity 99.9%, SIGMA ALDRICH
1.5 TiO2, purity 99.9%, SIGMA ALDRICH
1.6 SiO2, purity 99.9%, Umicore
1.7 Flux ชนิด LiT49.75/LiM49.75/LiBr0.5
2. อุปกรณ์และเครื่องมือที่ใช้ในการเตรียมสารตัวอย่าง
2.1 บีกเกอร์
2.2 ช้อนตักสาร
2.3 โกร่งบดสาร
2.4 กระดาษชั่งสาร
2.5 Kapton holder และ kapton tape
2.6 Pellet Pressing Die ขนาดเส้นผ่านศูนย์กลาง 10 mm
2.7 Platinum Crucible และ Platinum Mold สำหรับขึ้นรูปชิ้นงาน
2.8 เครื่องเตรียมตัวอย่างอัตโนมัติระบบไฟฟ้า รุ่น K2 Prime Fluxer
3. วิธีการเตรียมสารมาตรฐานด้วยวิธีการหลอม (fusion method)
3.1 นำสารตั้งต้นกลุ่มออกไซด์มาทำการบดใน mortar ให้ละเอียด แล้วนำไป sieve ด้วยผ้าเพื่อที่จะทำให้สารตั้งต้นมีขนาดอนุภาคน้อยกว่า 100 µm เมื่อ sieve เสร็จจะนำสารไปเก็บไว้ในขวดเก็บสาร
3.2 ชั่งสารตั้งต้นตามสัดส่วนที่คำนวณ แสดงดังตารางที่ 1 ซึ่งในการเตรียมครั้งนี้ จะกำหนดปริมาณของสาร Fe2O3 ที่ปริมาณร้อยละ 0, 1, 3, 5, 9 และ 11 เปอร์เซ็นต์โดยน้ำหนักตามลำดับ และกำหนดสัดส่วนของสารตั้งต้นต่อฟลักซ์ช่วยหลอม ในอัตราส่วน 1:10 ตามลำดับ
ตาราง 1 แสดงปริมาณสารตั้งต้นสำหรับการเตรียมสารมาตรฐานโดยการกำหนดปริมาณ Fe2O3 ที่ปริมาณต่าง ๆ
| สารตั้งต้น (g) | 0% Fe | 1% Fe | 3 % Fe | 5 % Fe | 7 % Fe | 9 % Fe | 11 % Fe |
|---|---|---|---|---|---|---|---|
| SiO2 | 77.769 | 79.769 | 81.769 | 83.769 | 85.769 | 89.106 | 87.769 |
| K2O | 3.017 | 3.017 | 3.017 | 3.017 | 3.017 | 3.017 | 3.017 |
| CaO | 4.308 | 4.308 | 4.308 | 4.308 | 4.308 | 4.308 | 4.308 |
| TiO2 | 2.904 | 2.904 | 2.904 | 2.904 | 2.904 | 2.904 | 2.904 |
| Cr2O3 | 0.665 | 0.665 | 0.665 | 0.665 | 0.665 | 0.665 | 0.665 |
| Fe2O3 | 11.337 | 9.337 | 7.337 | 5.337 | 3.337 | 0 | 1.337 |
| Total (g) | 100 | 100 | 100 | 100 | 100 | 100 | 100 |
ตาราง 2 แสดงปริมาณสารตั้งต้นสำหรับการเตรียมสารมาตรฐานหลัง K2O ถูกคูณด้วยค่าประกอบโดยน้ำหนัก
| สารตั้งต้น (g) | 0% Fe | 1% Fe | 3 % Fe | 5 % Fe | 7 % Fe | 9 % Fe | 11 % Fe |
|---|---|---|---|---|---|---|---|
| SiO2 | 89.106 | 87.769 | 85.769 | 83.769 | 81.769 | 79.769 | 77.769 |
| K2CO3 | 4.43499 | 4.43499 | 4.43499 | 4.43499 | 4.43499 | 4.43499 | 4.43499 |
| CaO | 4.808 | 4.808 | 4.808 | 4.808 | 4.808 | 4.808 | 4.808 |
| TiO2 | 2.904 | 2.904 | 2.904 | 2.904 | 2.904 | 2.904 | 2.904 |
| Cr2O3 | 0.665 | 0.665 | 0.665 | 0.665 | 0.665 | 0.665 | 0.665 |
| Fe2O3 | 0 | 1.337 | 3.337 | 5.337 | 7.337 | 9.337 | 11.337 |
| Total (g) | 101.418 | 101.418 | 101.418 | 101.418 | 101.418 | 101.418 | 101.418 |
ตาราง 3 แสดงปริมาณสารตั้งต้นสำหรับการเตรียมสารตัวอย่างที่สัดส่วน sample: flux เท่ากับ 1: 10
| สารตั้งต้น (g) | 0% Fe | 1% Fe | 3 % Fe | 5 % Fe | 7 % Fe | 9 % Fe | 11 % Fe |
|---|---|---|---|---|---|---|---|
| SiO2 | 0.559110 | 0.550721 | 0.538172 | 0.525622 | 0.513073 | 0.500524 | 0.487974 |
| K2CO3 | 0.027828 | 0.027828 | 0.027828 | 0.027828 | 0.027828 | 0.027828 | 0.027828 |
| CaO | 0.027031 | 0.027031 | 0.027031 | 0.027031 | 0.027031 | 0.027031 | 0.027031 |
| TiO2 | 0.018222 | 0.018222 | 0.018222 | 0.018222 | 0.018222 | 0.018222 | 0.018222 |
| Cr2O3 | 0.004173 | 0.004173 | 0.004173 | 0.004173 | 0.004173 | 0.004173 | 0.004173 |
| Fe2O3 | 0 | 0.008389 | 0.020939 | 0.033488 | 0.046037 | 0.058587 | 0.071136 |
| Sum of sample (g) | 0.636364 | 0.636364 | 0.636364 | 0.636364 | 0.636364 | 0.636364 | 0.636364 |
| Flux (g) | 6.363636 | 6.363636 | 6.363636 | 6.363636 | 6.363636 | 6.363636 | 6.363636 |
| Total (g) | 7 | 7 | 7 | 7 | 7 | 7 | 7 |





1. ผลการวิเคราะห์ฟลูออเรสเซนต์สเปคตรัมของสารมาตรฐานที่ถูกเตรียมด้วยวิธีหลอม (fusion method) และวิธีอัดเม็ด (pressed powder)
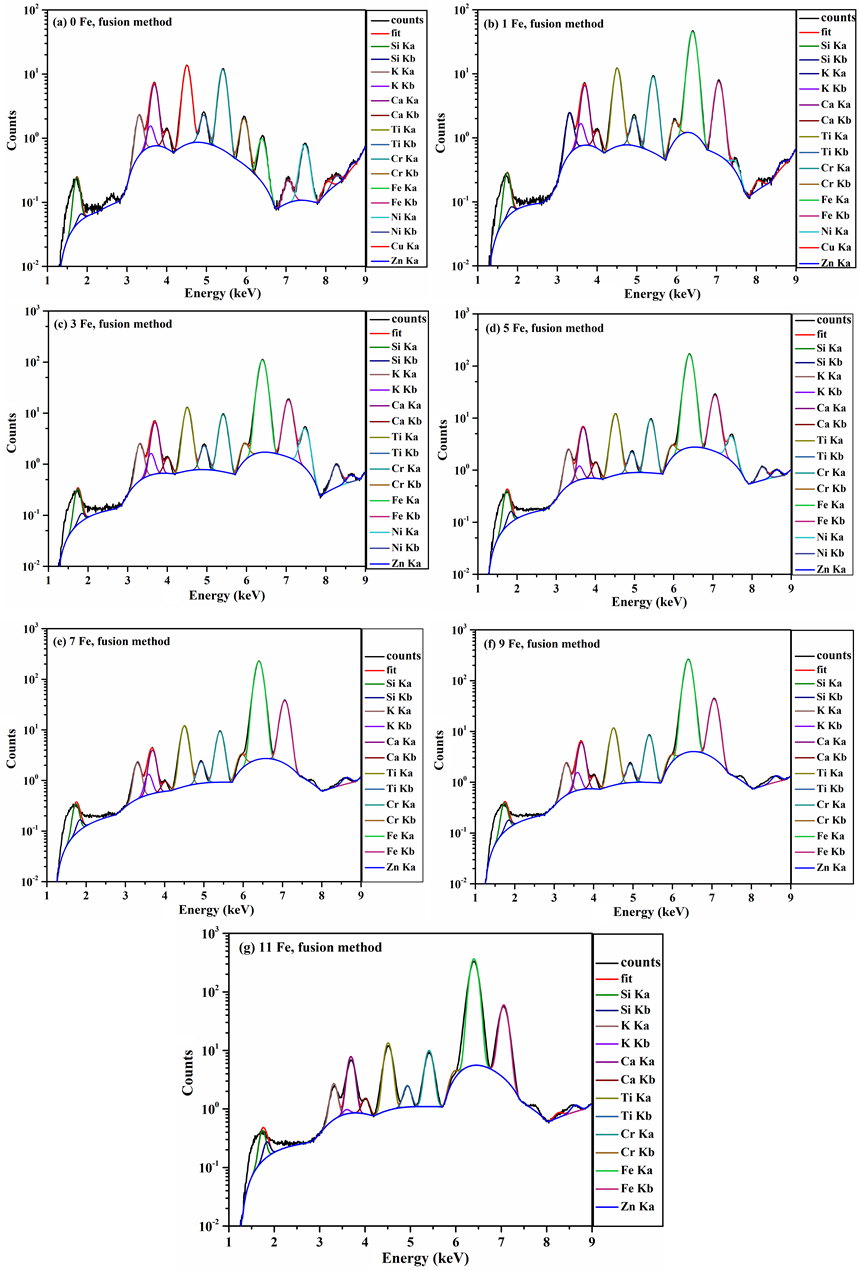
จากผลการวิเคราะห์ฟลูออเรสเซนต์สเปคตรัมของสารมาตรฐานที่ถูกกำหนดปริมาณ Fe2O3 ที่ปริมาณร้อยละ 0−11 โดยมวล ซึ่งการเตรียมด้วยวิธีการหลอม (fusion method) แสดงดังรูปที่ 8 (a−g) พบว่าองค์ประกอบของธาตุที่เกิดขึ้นในฟลูออเรสเซนต์สเปคตรัม จะมีค่าพลังงานสอดคล้องกับชนิดของธาตุที่ใช้เป็นสารตั้งต้นในการเตรียมสารมาตรฐาน นั่นคือธาตุ Si, K, Ca, Ti, Cr และ Fe นอกจากนี้เกิดพีคแปลกปลอมของธาตุอื่นในฟลูออเรสเซนต์สเปคตรัม เช่น พีคของ Ni, Cu และ Zn ตามลำดับ
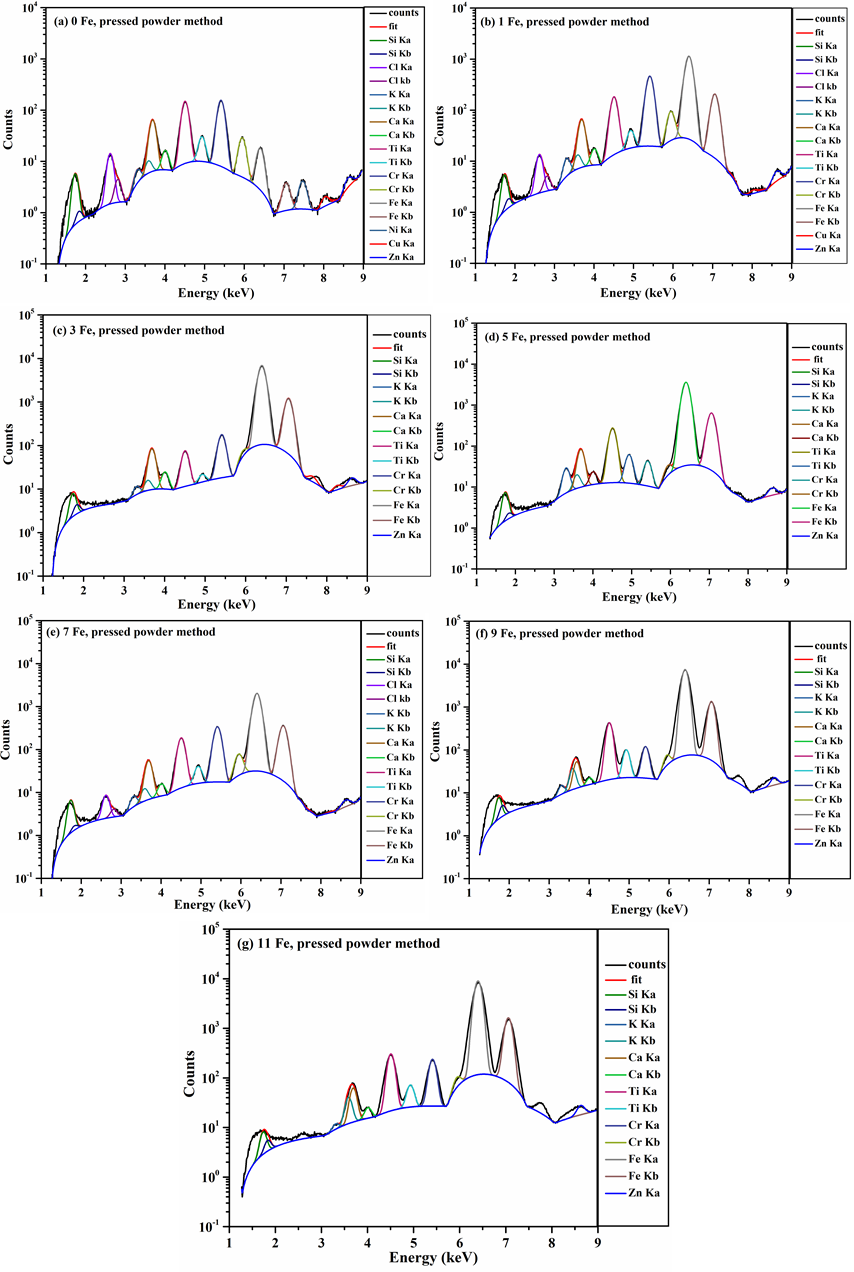
ซึ่งสามารถอธิบายได้ว่า พีคของธาตุดังกล่าวอาจเกิดจาก trace element ของสารประกอบ SiO2 ที่ใช้ในการเตรียมสารมาตรฐาน ในขณะเดียวกัน ผลการวิเคราะห์ฟลูออเรสเซนต์สเปคตรัมของสารมาตรฐานที่เตรียมด้วยวิธีอัดเม็ด (press powder method) แสดงดังรูปที่ 9 (a−g) พบว่าพีคที่เกิดขึ้นมีค่าพลังงานสอดคล้องกับชนิดธาตุที่ใช้ในการเตรียมสารมาตรฐานเช่นกัน และเกิดพีคที่สันนิษฐานว่าอาจเกิดจาก trace element ของสารประกอบ SiO2 หรือจากการปนเปื้อนในระหว่างการเตรียม
นั่นคือจะพบพีคของธาตุ Cl, Ni, Cu และ Zn ตามลำดับ ดังนั้นสามารถสรุปผลการวิเคราะห์ในเชิงคุณภาพได้ว่า องค์ประกอบของธาตุส่วนใหญ่ที่เกิดขึ้นในฟลูออเรสเซนต์สเปคตรัมของสารมาตรฐานที่ถูกเตรียมด้วยวิธีทั้งสองแบบนั้น จะมีค่าพลังงานที่สอดคล้องกับชนิดของธาตุที่ใช้เป็นสารตั้งต้น และอาจมีองค์ประกอบของธาตุอื่น ๆ ที่เกิดจาก trace element ในสารประกอบ SiO2 ที่ใช้เตรียมเป็นสารตั้งต้นในปริมาณเล็กน้อย
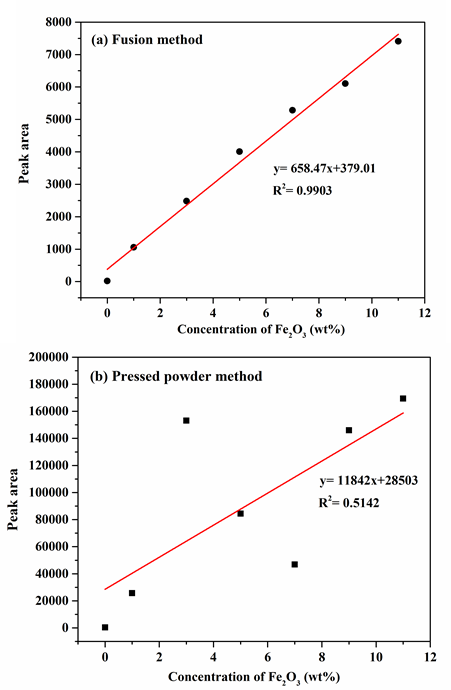
จากผลการทดลองสามารถสรุปผลการวิเคราะห์เชิงคุณภาพได้ว่า องค์ประกอบของธาตุส่วนใหญ่ในสารมาตรฐานที่ถูกเตรียมด้วยวิธีการหลอม และอัดเม็ด จะมีค่าพลังงานที่สอดคล้องกับชนิดของธาตุที่ใช้เป็นสารตั้งต้น และอาจมีองค์ประกอบของธาตุอื่น ๆ ที่เกิดจาก trace element ในสารประกอบที่ใช้เตรียมเป็นสารตั้งต้นในปริมาณเล็กน้อย ในขณะที่ผลการวิเคราะห์เชิงปริมาณพบว่า วิธีการเตรียมสารมาตรฐานที่ต่างวิธีนั้นจะส่งผลต่อลักษณะของ calibration curve โดยวิธีการหลอมอาจเป็นวิธีที่ใช้เวลาในการเตรียมนาน แต่จะได้สารมาตรฐานที่มีความสม่ำเสมอ และมีความเป็นเนื้อเดียวกันสูง ซึ่งจะส่งผลให้ calibration curve มีความน่าเชื่อถือ และเป็นไปตามทฤษฏี ในขณะเดียวกันการเตรียมสารตัวอย่างด้วยวิธีอัดเม็ดนั้นเป็นวิธีที่ทำได้ง่ายและรวดเร็ว แต่อาจจะได้สารมาตรฐานที่ไม่มีความเป็นเนื้อเดียวกัน และอนุภาคมีความไม่สม่ำเสมออันเนื่องมาจากขั้นตอนการบดผสมสารที่ไม่ดีพอ รวมไปถึงเม็ดอัดอาจมีผิวหน้าที่ไม่เรียบ จึงส่งผลให้เกิดการกระเจิงของรังสีเอกซ์ที่แตกต่างกัน ทำให้ผล calibration curve ไม่น่าเชื่อถือและไม่เป็นไปตามทฤษฎี